Метаболизм фруктозы и галактозы
Фруктоза и галактоза наряду с глюкозой используются для получения энергии или синтеза веществ: гликогена, ТГ, ГАГ, лактозы и др.
Значительное количество фруктозы, образующееся при расщеплении сахарозы, превращается в глюкозу уже в клетках кишечника. Часть фруктозы поступает в печень.
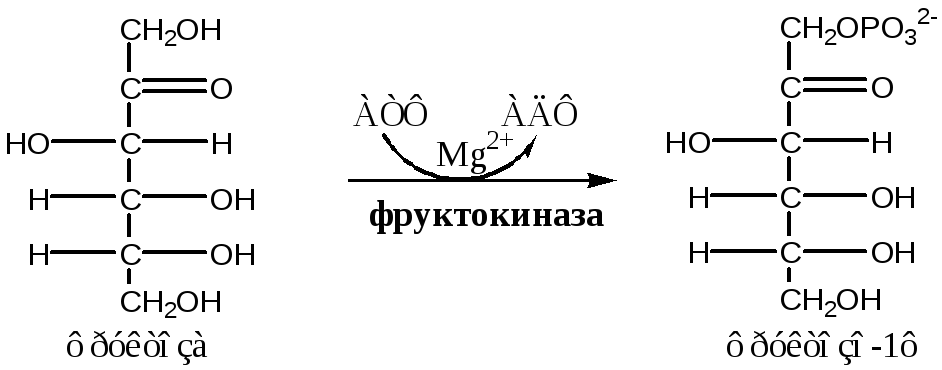
Метаболизм фруктозы в клетке начинается с реакции фосфорилирования:
1.Фруктокиназа(АТФ: фруктоза-1-фосфотрансфераза) фосфорилирует только фруктозу, имеет к ней высокое сродство. Содержится в печени, почках, кишечнике. Инсулин не влияет на ее активность.
2. Альдолаза В(фруктозо: ГА-лиаза) есть в печени, расщепляет фруктозо-1ф (фруктозо-1,6ф) до глицеринового альдегида (ГА) и диоксиацетонфосфата (ДАФ).
3.Триозокиназа(АТФ: ГА-3-фосфотрансфераза). Много в печени.
ДАФ и ГА, полученные из фруктозы, включаются в печени главным образом в глюконеогенез. Часть ДАФ может восстанавливаться до глицерол-3-ф и участвовать в синтезе ТГ.
Нарушения метаболизма фруктозы
Причиной нарушения метаболизма фруктозы является дефект ферментов.
Доброкачественная эссенциальная фруктозурия связана с недостаточностью фруктокиназы,клинически не проявляется. Фруктоза накапливается в крови и выделяется с мочой, где её можно обнаружить лабораторными методами. Частота 1:130 000.
Наследственная непереносимость фруктозычастая патология, возникает при генетически дефектеальдолазы В(аутосомно-рецессивная форма). Она проявляется, когда в рацион добавляют фрукты, соки, сахарозу. После приёма пищи, содержащей фруктозу возникаетрвота, боли в животе, диарея, гипогликемия и даже кома и судороги. У маленьких детей и подростков развиваютсяхронические нарушения функций печени и почек. Болезнь сопровождаетсянакоплением фруктозо-1-ф,который ингибирует активность фосфоглюкомутазы, поэтому происходит торможение распада гликогена и развиваетсягипогликемия. Как следствие, ускоряется мобилизация липидов, окисление жирных кислот и синтез кетоновых тел. Повышение кетоновых тел может привести к метаболическому ацидозу.
Результатом торможения гликогенолиза и гликолиза является снижение синтеза АТФ. Кроме того, накопление фосфорилированной фруктозы ведёт к нарушению обмена неорганического фосфата и гипофосфатемии. Для пополнения внутриклеточного фосфата ускоряется распад адениловых нуклеотидов. Продукты распада этих нуклеотидов включаются в катаболизм, проходя стадии образования гипоксантина, ксантина и, наконец, мочевой кислоты. Повышение количества мочевой кислоты и снижение экскреции уратов в условиях метаболического ацидоза проявляются в видегиперурикемии. Следствием гиперурикемии может быть подагра даже в молодом возрасте.
Галактоза образуется в кишечнике в результате гидролиза лактозы. Превращение галактозы в глюкозу происходит в печени в реакции эпимеризации в виде УДФ-производного.
Галактокиназа(АТФ: галактозо-1-фосфотрансфераза) фосфорилирует галактозу.
Галактозо-1ф-уридилтрансферазазамещает галактозой остаток глюкозы в УДФ-глюкозе с образованием УДФ-галактозы.
Эпимераза(УДФ-галактозо-УДФ-глюкозо-изомераза) — НАД-зависимый фермент, катализирует эпимеризацию ОН группы по С4углеродному атому, обеспечивая взаимопревращения галактозы и глюкозы в составе УДФ.
Образованная глюкозо-1-ф может включаться в: 1) синтез гликогена; 2) превращение в свободную глюкозу; 3) катаболизм, сопряжённый с синтезом АТФ, и т.д.
Нарушения метаболизма галактозы
Галактоземияобусловленна наследственным дефектом любого из трёх ферментов, включающих галактозу в метаболизм глюкозы.
Галактоземия, вызванная недостаточностью галактозо-1-фосфатуридилтрансферазы (ГАЛТ) имеет несколько форм, проявляется рано, и особенно опасна для детей, так как материнское молоко, содержит лактозу. Ранние симптомы дефекта ГАЛТ:рвота, диарея, дегидратация, уменьшение массы тела, желтуха. В крови, моче и тканях повышается концентрация галактозы и галактозо-1-ф. В тканях глаза (в хрусталике) галактоза восстанавливается альдоредуктазой (НАДФ) с образованием галактитола (дульцита). Галактитол накапливается в стекловидном теле и связывает большое количество воды, чрезмерная гидратация хрусталика приводит к развитию катаракты, которая наблюдается уже через несколько дней после рождения. Галактозо-1-ф ингибирует активность ферментов углеводного обмена (фосфоглюкомутазы, глюкозо-6-фосфатдегидрогеназы).
Галактозо-1ф оказывает токсическое действие на гепатоциты: возникают гепатомегалия, жировая дистрофия. Галактитол и галактозо-1-ф вызывают почечную недостаточность. Отмечают нарушения в клетках полушарий головного мозга и мозжечка, в тяжёлых случаях — отёк мозга, задержку умственного развития, возможен летальный исход.
Некоторые дефекты в строении ГАЛТ приводят лишь к частичной потере активности фермента. Поскольку в норме ГАЛТ присутствует в организме в избытке, то снижение его активности до 50%, а иногда и ниже может клинически не проявляться.
Лечение заключается в удалении галактозы из рациона.
Педфак. Особенности катаболизма моносахаридов у новорожденных и детей.
У детей активен УДФ-глюкоза ↔ УДФ-галактоза путь. У взрослых этот путь неактивен. У новорожденных низкая активность ПФШ. При рождении у ребенка происходит переключение катаболизма глюкозы с анаэробного на аэробный путь. Вначале преобладает использование липидов.
Источник
2.1.3.2. Начальный этап метаболизма фруктозы
Фруктоза также после поступления в клетки подвергается фосфорилированию с использованием в качестве фосфорилирующего агента АТФ. Реакция катализируется ферментом фруктокиназай. Образовавшийся Фр-1-ф расщепляется на глицериновый альдегид и фосфогидроксиацетон ( ФГА ) при участии фермента фруктозо-1-фосфатальдолазы . Глицериновый альдегид при участии фермента триозокиназы превращается в 3-фосфоглицериновый альдегид, в ходе фосфорилирования используется молекула АТФ, переходящая в АДФ. Фосфогидроксиацетон при участии триозофосфатизомеразы также превращается в 3-фосфоглицериновый альдегид. Таким образом, из молекулы фруктозы получается 2 молекулы 3-фосфоглицеринового альдегида, а 3-ФГА является промежуточным метаболитом окислительного расщепления глюкозы.
Возможен другой вариант начального этапа метаболизма фруктозы. В этом случае фруктоза подвергается фосфорилированию при участии фермента гексокиназы с образованием фруктозо-6-фосфата с использованием в качестве фосфорилирующего агента АТФ. Однако способность гексокиназы фосфорилировать фруктозу сильно ингибируется в присутствии глюкозы, поэтому считается маловероятным, чтобы этот вариант использования фруктозы играл сколь-либо существенную роль в ее метаболизме.
2.1.3.3. Начальный этап метаболизма гликогена
Окислительное расщепление остатков глюкозы из молекулы гликогена чаще всего начинается с его фосфоролитического расщепления: при участии фермента фосфорилазы с использованием неорганического фосфата от молекулы гликогена последовательно отщепляются моносахаридные блоки с образованием глюкозо-1-фосфата. Гл-1-ф при участии фосфоглюкомутазы превращается в гл-6-Ф — метаболит окислительного пути расщепления глюкозы. Такой путь использования гликогена характерен для клеток мышц или печени.
Для клеток мозга или кожи преобладающим является амилолитический путь расщепления гликогена: вначале под действием ферментов амилазы и мальтазы гликоген расщепляется до свободной глюкозы, а затем глюкоза фосфорилируется и подвергается дальнейшему окислению уже известным нам путем.
2.1.4. Анаэробный метаболизм углеводов
Человек является аэробным организмом, так как основным конечным акцептором отщепляемых от окисляемых субстратов атомов водорода является кислород. Парциальное давления кислорода в тканях составляет в среднем 35-40 мм рт. ст. Но это вовсе не значит, что при определенных условиях в тканях не возникает дефицит кислорода, делающий невозможным протекание аэробных окислительных процессов. Торможение окислительных процессов при дефиците кислорода связано с тем, что клеточный пул НАД+ и других коферментов. способных акцептировать атомы водорода от окисляемых субстратов, весьма ограничен. Как только основная их масса переходит в восстановленное состояние из-за дефицита кислорода, дегидрирование субстратов прекращается. Развивается гипоэнергетическое состояние, которое может стать причиной гибели клеток.
В подобного рода условиях в клетках различных органов и тканей включаются механизмы, обеспечивающие клетки энергией, не зависящие от наличия кислорода. Основными из них являются анаэробное окисление глюкозы — анаэробный гликолиз, и анаэробное расщепление гликогена — гликогенолиз. В анаэробных условиях расщепление глюкозы и гликогена идет абсолютно идентичными по сравнению с ранее рассмотренными нами метаболическими путями вплоть до образования пирувата. Однако далее эти пути расходятся: если в аэробных условиях пируват подвергается окислительному декарбоксилированию, то в анаэробных условиях пировиноградная кислота восстанавливается в молочную кислоту. Реакция катализируется ферментом лактатдегидрогеназой:
Разумеется, расщепление глюкозы до лактата сопровождается высвобождением лишь 1/12 — 1/13 всей заключенной в химических связях глюкозы энергии ( ~ 50 ккал/моль ), тем не менее на каждую распавшуюся в ходе анаэробного гликолиза молекулу глюкозы клетка получает 2 молекулы АТФ (2 АТФ расходуется и 4 АТФ синтезируется). При гликогенолизе клетка получит 3 молекулы АТФ на каждый остаток глюкозы из молекулы гликогена ( 1 АТФ расходуется и 4 АТФ синтезируется ). Несмотря на очевидную невыгодность в отношении количества высвобождаемой энергии анаэробные гликолиз и гликогенолиз позволяют клеткам существовать в условиях отсутствия кислорода. Анаэробный путь окисления глюкозы и анаэробное расщепление гликогена играют важную роль в обеспечении клеток энергией, вопервых, в условиях высокой экстренно возникающей функциональной нагрузки на тот или иной орган или организм в целом, примером чего может служить бег спортсмена на короткую дистанцию. Во-вторых, эти процессы играют большую роль в обеспечении клеток энергией при гипоксичеких состояниях, например, при тромбозах артерий в период до развития коллатерального кровообращения или при тяжелых шоковых состояниях с выраженными расстройствами гемодинамики.
Активация анаэробного окисления углеводов приводит к увеличению продукции лактата в клетках и тканях. При сохранении кровообращения этот наработанный в клетках лактат выносится кровью и основная его часть метаболизируется в печени или в сердечной мышце. В миокарде лактат окисляется до углекислого газа и воды; в печени же лишь примерно 1/5 поступающего лактата подвергается окислению до конечных продуктов, а 4/5 — ресинтезируются в глюкозу в ходе интенсивно идущего в печени процесса глюконеогенеза.
Если же вынос лактата из гипоксической ткани невозможен, то при его накоплении в клетках за счет повышения концентрации протонов ингибируется фосфофруктокиназа, в результате чего ингибируются и гликолиз, и гликогенолиз. Клетки, лишенные последних источников энергии, обычно погибают, что наблюдается при инфарктах различных органов, в особенности при инфаркте миокарда.
Следует заметить, что в клетках некоторых органов и тканей человека образование молочной кислоты происходит и в обычных, т.е. в аэробных условиях. Так. в эритроцитах, не имеющих митохондрий. все необходимое для них количество энергии вырабатывается в ходе гликолиза. К тканям с относительно высоким уровнем аэробного гликолиза относятся также сетчатка глаза и кожа. Высокий уровень аэробного гликолиза присущ также многим опухолям.
Биосинтетические процессы, протекающие в клетках, нуждаются не только в энергии, им необходимы также восстановительные эквиваленты в виде НАДФН+Н+и целый ряд моносахаридов, имеющих в своем составе пять атомов углерода,такие как рибоза,ксилоза и др.Образование восстановленного НАДФ идет в пентозном цикле окисления углеводов, а образование пентоз может происходить как в пентозном цикле окисления, так и в других метаболических путях.
Источник