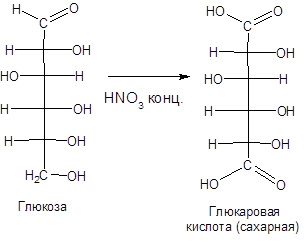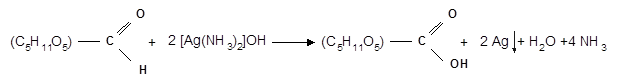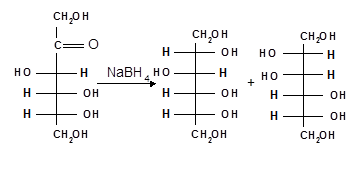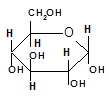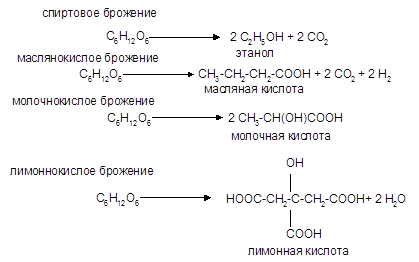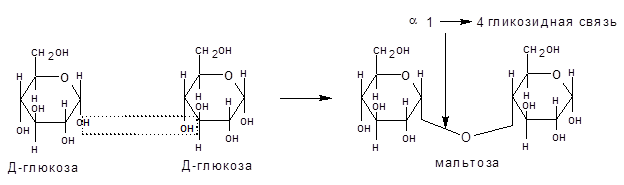- Химические свойства моносахаридов. В соответствии с химическим строением моносахариды могут проявлять свойства карбонильных соединений
- 1. Реакции карбонильных форм моносахаридов
- 2. Реакции с участием гидроксильных групп
- 3. Брожение сахаров
- Перечислите ,пожалуйста ,химические свойства фруктозы:по порядку(если возможно с уровнениями реакций)
- Вариант №7-кислород -Нагорная, Никитин, Овдиенко
Химические свойства моносахаридов. В соответствии с химическим строением моносахариды могут проявлять свойства карбонильных соединений
В соответствии с химическим строением моносахариды могут проявлять свойства карбонильных соединений, спиртов и полуацеталей. Поскольку циклические и открытые формы моносахаридов в растворе находятся в равновесии друг с другом, то расходование одной из них в ходе реакции сдвигает таутомерное равновесие в сторону реагирующей формы. Рассматривая различные реакции моносахаридов, мы будем приводить формулу лишь той таутомерной формы, которая непосредственно участвует в данной реакции.
1. Реакции карбонильных форм моносахаридов
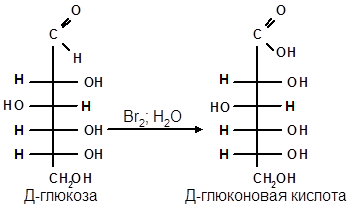
а) Окисление. Реакции окисления используют в структурных исследованиях и биохимических анализах для обнаружения моносахаридов. Монозы легко окисляются, причем в зависимости от условий окисления образуются различные продукты.
Пример окисления глюкозы:
С помощью сильного окислителя — концентрированной азотной кислоты — концевые группы альдоз (альдегидная и первичноспиртовая) одновременно окисляются в карбоксильные группы, образуя гликаровые кислоты (называемые также сахарными):
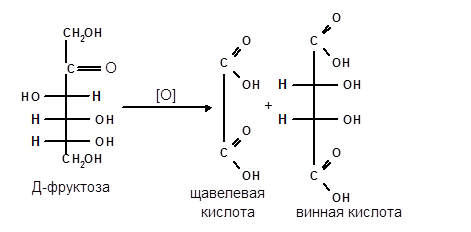
Кетозы не окисляются слабыми окислителями. При действии сильных окислителей происходит расщепление молекул. Так, например, при окислении фруктозы получаются винная и щавелевая кислоты:
Слабые окислители в щелочной среде (аммиачный раствор оксида серебра, соединения Сu 2+ ) превращают монозы в сложную смесь продуктов окисления и служат для качественного и количественного определения альдоз и кетоз.
Подобно обычным альдегидам, альдозы легко дают реакцию “серебряного зеркала” с аммиачным раствором оксида серебра (реактив Толленса):
Кетозы тоже способны восстанавливать катионы металлов, так как они в щелочной среде изомеризуются в альдозы.
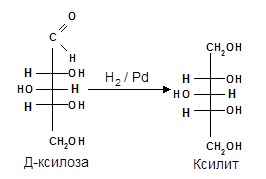
б) Восстановление. При восстановлении моноз образуются многоатомные спирты, называемые альдитами (глицитами). Эти кристаллические, легко растворимые в воде вещества обладают сладким вкусом и часто используются как заменители сахара (ксилит, сорбит).
Простейшим сахароспиртом является трехатомный спирт глицерин, образующийся при восстановлении глицеральдегида. Глюкоза при восстановлении дает шестиатомный сахароспирт сорбит, галактоза – дульцит, манноза – манит:
Сорбит часто встречается в различных фруктах, ягодах: в рябине, сливах, абрикосах, вишнях и др. Дульцит содержится во многих растениях, выделяется на поверхности коры деревьев. Манит содержится в бурых водорослях; плодах (ананас), овощах (морковке, луке).
Восстановление моносахаридов проводят водородом в присутствии металлических катализаторов (палладий, никель).
Шестиатомные спирты — глюцит (сорбит), дульцит и маннит — получаются при восстановлении соответственно глюкозы, галактозы и маннозы. Восстановление глюкозы в сорбит является одной из стадий промышленного синтеза аскорбиновой кислоты.
При восстановлении альдоз получается лишь один полиол, кетоз — смесь двух полиолов, например, при восстановлении Д-фруктозы борогидридом натрия NaBН4 образуются Д- глюцит (сорбит) и Д-маннит:
| Д-фруктоза | Д-глюцит | Д-маннит |
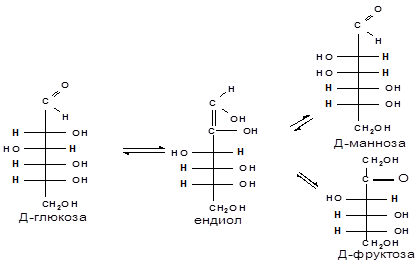
в) Действие щелочей. В разбавленных растворах щелочей при комнатной температуре происходит изомеризация моносахаридов, т.е. получение из одного моносахарида равновесной смеси моноз, отличающихся конфигурацией первого и второго атомов углерода.
Так, водный раствор Д-глюкозы после добавления к нему известковой воды через пять суток имеет состав: Д-глюкозы — 63,5 %, Д-маннозы — 2,5 % и Д-фруктозы — 31 %. Процесс изомеризации проходит через стадию образования промежуточного продукта — ендиола, который для глюкозы, маннозы и фруктозы является общим:
2. Реакции с участием гидроксильных групп
Гидроксильные группы имеются в открытых и циклических формах моноз, но содержание циклических форм значительно выше, поэтому реакции идут в циклических (полуацетальных) формах:
Гидроксилы отличаются по реакционной способности: С1-ОН-гликозидный (наиболее реакционноспособный); С6 — первичный; С2-С4 — вторичные.
2.1 Реакции с участием гликозидного гидроксила
При взаимодействии моносахаридов с гидроксилсодержащими соединениями (спиртами, фенолами и др.) в условиях кислотного катализа образуются производные только по гликозидной ОН-группе — циклические ацетали, называемые гликозидами. Cпиртовые гидроксилы моноз в этих условиях не реагируют.
Удобным способом получения гликозидов является пропускание газообразного хлороводорода (катализатор) через раствор моносахарида в спиртах, например, этаноле, метаноле и т.д. При этом соответственно получаются этил- или метилгликозиды. В названии гликозидов указываются сначала наименования введенного радикала, затем конфигурация аномерного центра и название углеводного остатка с суффиксом — озид.
3. Брожение сахаров
Брожение — это сложный процесс расщепления моносахаридов с выделением СО2 под действием ферментов. Брожению подвергаются сахара, у которых число атомов углерода кратно трем (гексозы).
Брожение гексоз различной конфигурации происходит с неодинаковой легкостью. Существуют и другие виды брожения.
Процессы брожения сахаров играют важную роль и широко используются в промышленности.
Различают разные виды брожения:
Гликозидная связь имеет очень важное биологическое значение. С помощью этой связи осуществляется ковалентное связывание моносахаридов в составе олиго- и полисахаридов:
Понравилась статья? Добавь ее в закладку (CTRL+D) и не забудь поделиться с друзьями:
Источник
Перечислите ,пожалуйста ,химические свойства фруктозы:по порядку(если возможно с уровнениями реакций)
Фруктоза, или плодовый сахар C6H12O6 — моносахарид, который в свободном виде присутствует почти во всех сладких ягодах и плодах. Фруктоза имеет такую же, как и глюкоза, молекулярную формулу (С6Н12О6), но является не полиоксиальдегидом, а полиоксикетоном. Молекула фруктозы содержит три асимметрических атома углерода, причем конфигурация у них такая же, как и у соответствующих атомов в молекуле глюкозы. Итак, фруктоза — изомер и «близкий родственник» глюкозы. Она хорошо растворима в воде, имеет сладкий вкус (примерно в 3 раза слаще глюкозы) . Фруктозе свойственны многие реакции, свойственные глюкозе (образование полиэфиров, брожение)
Фруктоза также наиболее часто встречается в циклических формах (альфа — или бета-), но, в отличие от глюкозы, в пятичленных. В водных растворах фруктозы имеет место равновесие:
Фруктоза дает общие р-ции на кетозы, проявляет восстанавливающие св-ва, образует ряд характерных производных благодаря карбонильной группе, в частности фенилозазон (II), идентичный фенилозазонам глюкозы и маннозы.
При восстановлении карбонильной группы фруктозы образуются сорбит и маннит.
Фруктоза не устойчива в щелочах и к-тах и может полностью разрушаться в условиях кислотного гидролиза полисахаридов или гликозидов (напр. , при нагр. с 2 н. H2SO4 при 100оC в течение неск. часов) , при котором обычные альдозы не подвергаются деструкции.
Проба Селиванова — качественное обнаружение фруктозы. При нагревании пробы с фруктозой в присутствии резорцина и соляной кислоты появляется вишнево-красное окрашивание.
Источник
Вариант №7-кислород -Нагорная, Никитин, Овдиенко
1. Сахароза не вступает в реакцию: а) этерификации; б) серебряного зеркала; в) с Сu(ОН)2; г) гидролиза.
2. Осуществимы реакции: а) гидролиза глюкозы ;б) гидрирования фруктозы; в) полимеризации глюкозы; г) спиртового брожения глюкозы; д) молочнокислого брожения целлюлозы; е) окисления глюкозы аммиачным раствором оксида серебра.
3. О целлюлозе можно сказать, что: это полимер, образованный остатками α-глюкозы, связанными гликозидными связями; б) ее молекулы имеют как линейное , так и разветвленное строение; в) между ее молекулами образуется множество водородных связей, благодаря чему притяжение между молекулами сильное; г) организм человека не содержит ферментов, необходимых для ее гидролиза; д) она окисляется гидроксидом меди (II); е) она может образовывать простые и сложные эфиры.
4. Реакция «серебряного зеркала» является характерной для: а) ненасыщенных углеводных; б) карбоновых кислот; в) ненасыщенных спиртов ;г) альдегидов.
5. Реакцией эстерификации называется: а) образование эстера из карбоновой кислоты и спирта; б) получение эстера в результате реакции дегидратации; в) взаимодействие эстера с водой ;г) взаимодействие насыщенных карбоновых кислот с галогенами.
Вариант №8-кислород -Африка-Солдатенко, Ткаченко, Бабичева
1. Выбрать неверное утверждение: а) уксусная кислота может образовывать уксусный ангидрид; б) уксусная кислота не взаимодействует с аммиаком; в) уксусная кислота выходит окислением бутана; г) уксусная кислота взаимодействует с магнием.
2. Качественной реакцией на многоатомные спирты является: а) реакция дегидратации; б) их взаимодействие с купрум гидроксидом; б) характерный окрас пламени; г) их взаимодействие с солями серебра.
3. Записи СН3-СН2-СНОН-СН3 и СН3-СН2-О-СН3 отражают строение: а) веществ разных классов, не являющихся изомерами; б) одного и того же вещества; в) гомологов; г) изомеров.
4. Оцените справедливость утверждений: 1) температуры кипения спиртов ниже, чем у соответствующих алканов; 2) водородные связи образуются между молекулами, содержащими протонизированные атомы водорода;а)верно только 1; б) верно только 2; в) оба утверждения верны; г) оба утверждения неверны.
5. Метанол не вступает в реакцию: а) внутримолекулярной дегидратации; б) межмолекулярной дегидратации; в) этерификации; г) окисления.
Вариант №9-кислород -Пискарева, Слащилин, Ткаченко
1. Количество вещества кислорода, необходимого для полного сгорания 1 моль бутанола, равно: а) 12; б) 6,5; в) 6; г) 4.
2. Реакция характерная для спиртов: а) присоединение хлора; б) дегидрирование; в) замещение атомов Гидрогена металлическими элементами; г) взаимодействие с алюминий хлоридом.
3. Какое вещество необходимо для получения этанола с хлорэтаном: а) натрий гидроксид; б) сульфатная кислоат; в) хлор; г) кислород.
4. Какое неароматическое соединение содержит гидроксигруппу: а) этанол; б) бензен; в) фенол; г) этаналь.
5. Общий признак между этанолом и этиленгликолем: а) при нормальных условиях пребывают в твердом состоянии; б) взаимодействуют с натрием; в) содержат в составе две гидроксигруппы ;г) взаимодействуют с натрий гидроксидом.
Вариант №10-кислород -Бутова, Логвиненко, Мамедова
1. Какой из спиртов проявляет чрезвычайную токсичность: а) этиловый ;б) метиловый; в) пропиловый; г) пентиловый.
2. Гексаналь и 2-метилбутен-2-ол-1 это названия: а) гомологов; б) изомеров; в) одного и того же вещества; г) веществ разных классов, не являющихся изомерами.
3. Пентаналь образуется окислением: а) пентанола-1; б) пентанола-2; в) пентина-1; г) пентена-1.
4. Пропановую кислоту можно получить из пропаноля в результате реакции его с: а) водородом; б) фенолом; в) гидроксидом меди (II); г) водой.
5. Про ацетальдегид можно сказать, что: а) он получается в реакции Кучерова ;б) он образуется при окислении этанола; в) он не вступает в реакции присоединения; г) это сырье для производства уксусной кислоты ;д) в его молекуле имеется сопряженная электронная система; е) в реакции серебряного зеркала он выступает в роли окислителя.
Вариант №11-кислород -Ковалева, Полищук, Селихова Настя
1. Какое ароматическое соединение содержит гидроксигруппу: а) этанол; б) бензен; в) фенол; г) толуэн.
2. С помощью какого вещества можно определить фенол в растворе: а) фенолфталеин; б) гидроген пероксид; в) феррум(III) хлорид; г) глицерин.
3. Какое вещество реагирует с натрий гидроксидом: а) фенол; б) этанол; в) пропанол; г) толуэн.
4. Общий признак между этанолом и фенолом: а) взаимодействуют с натрием; б) взаимодействуют с натрий гидроксидом; в) содержат в составе две гидроксигруппы; г) при нормальных условиях пребывают в твердом состоянии.
5. В каком агрегатном состоянии при обычных условиях существует фенол: а) плазма; б) жидкость; в) твердое вещество; г) газообразное вещество.
Дата добавления: 2021-05-18 ; просмотров: 296 ; Мы поможем в написании вашей работы!
© 2014-2023 — Студопедия.Нет — Информационный студенческий ресурс. Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав (0.013)
Источник