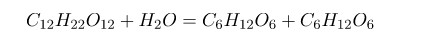- Химические свойства полисахаридов
- Опыт 9. Окисление моносахаридов бромной водой (тяга!).
- Опыт 11. Осмоление моносахаридов под действием щелочи.
- Химические свойства фруктозы. Получение. Применение
- Лекция Углеводы. Химические свойства
- Восстановление
- Окисление
- Мягкое окисление. Гликоновые кислоты
- Восстанавливающие моносахариды. Качественная реакция на альдегидную группу
- Жесткое окисление. Гликаровые кислоты
- Ферментативное окисление в организме. Гликуроновые кислоты
- Реакции полуацетального гидроксила. Гликозиды
- Строение гликозидов
- Получение гликозидов
- Гидролиз гликозидов
- Образование простых эфиров
- Образование сложных эфиров
- Дегидратация
Химические свойства полисахаридов
Углеводы объединяют разнообразные соединения – от низкомолекулярных, состоящих из нескольких атомов (х = 3), до полимеров [Сх(Н2О)у]n с молекулярной массой в несколько миллионов.
Классификация углеводов ( по числу молекул моносахаридов, образующихся при кислотном гидролизе углеводов):
1. Моносахариды (не подвергаются гидролизу): триозы, тетрозы, пентозы (рибоза С5Н10О5, дезоксирибоза С5Н10О4), гексозы (глюкоза, фруктоза – С6Н12О6)
2. Дисахариды (состоят из двух остатков молекул моносахаридов): сахароза, мальтоза, лактоза
3. Полисахариды (состоят из большого числа остатков молекул моносахаридов): крахмал, гликоген, целлюлоза, хитин
Моносахариды
Молекулярные формулы глюкозы и фруктозы совпадают: С6Н12О6. Следовательно, фруктоза и глюкоза являются структурными изомерами. Структурные формулы молекул этих моносахаридов показаны ниже:
Наряду с приведенными линейными (открытыми) формами глюкоза и фруктоза существуют в циклических α- и β-формах. Эти формы образуются за счет взаимодействия карбонильной и карбоксильной групп:
Физические и химические свойства глюкозы и фруктозы
Глюкоза (виноградный сахар) – бесцветное кристаллическое вещество, хорошо растворимое в воде, сладкое на вкус. Фруктоза – самый сладкий моносахарид, примерно вдвое слаже глюкозы.
Химические свойства глюкозы обусловлены наличием в молекуле альдегидной группы и пяти гидроксильных групп.
| Тип реакции | Примечание |
| Реакции с участием альдегидной группы | |
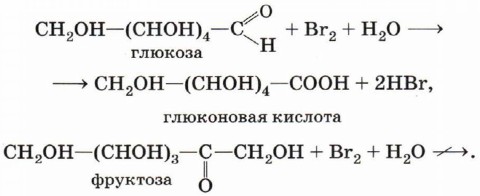
| Окисление: а) бромной водой СH2OH(CHOH)4-COH + Br2 + H2O → →СH2OH(CHOH)4-COOH + 2HBr глюконовая кислота б) аммиачным раствором Ag2O при слабом нагревании: СH2OH(CHOH)4-COH + Ag2O t.NH3 → →СH2OH(CHOH)4-COOH + 2Ag↓ в) свежеосажденным Cu(OH)2 при слабом нагревании: СH2OH(CHOH)4-COH + 2Cu(OH)2 t → →СH2OH(CHOH)4-COOH + Cu2O↓ + 2H2O | Реакцию с бромной водой используют для качественного определения альдегидной группы в молекуле глюкозы. Фруктоза бромную воду не обесцвечивает, т.е. с ней не реагирует. В эту же реакцию вступает и фруктоза, поскольку в щелочной среде изомеризуется в глюкозу Образуется красный осадок Cu2O. В подобную реакцию вступает и фруктоза |
| Восстановление: СH2OH(CHOH)4-COH + H2 t , Ni → СH2OH(CHOH)4-CH2OH сорбит | Под действием восстановителей глюкоза и фруктоза превращаются в шестиатомный спирт – сорбит |
| Реакции с участием гидроксильных групп | |
Взаимодействие с Cu(OH)2 при обычных условиях  | Появляется интенсивное синее окрашивание, что свидетельствует о наличии в молекуле глюкозы (фруктозы) нескольких гидроксильных групп |
| Взаимодействие с уксусной кислотой или уксусным ангидридом | Образуется сложный эфир глюкозы. В реакциях с галогеналканами образуются простые эфиры. В эти же реакции вступает и фруктоза |
Брожение 1.Спиртовое брожение: C6H12O6 → 2C2H5-OH + 2CO2↑ 2. Молочнокислое брожение:  |
Получение глюкозы
Источник
Опыт 9. Окисление моносахаридов бромной водой (тяга!).
В две пробирки наливают по 0,5 мл 1-2%-ных растворов глюкозы и фруктозы и добавляют в каждую пробирку по 3 мл бромной воды. Пробирки нагревают в кипящей водяной бане в течение15 минут. Если бурая окраска брома за это время не исчезает, то реакционные смеси кипятят до обесцвечивания в пламени горелки еще около 1 минуты.
После охлаждения к растворам добавляют по несколько капель 1%-ного раствора хлорида железа (Ш), окрашенного фенолом в фиолетовый цвет (к 3-4 мл 1%-ного раствора фенола добавляют несколько капель 1%-ного раствора хлорида железа (Ш)).
Сравните окраску растворов в обеих пробирках. Какой моносахарид – глюкоза или фруктоза – легче окисляется в условиях опыта?
Напишите уравнение реакции окисления глюкозы бромом в глюконовую кислоту.
Опыт 10. Реакция замещения карбонильного кислорода в моносахаридах
(получение фенилозазонов)
В пробирке смешивают 2,5 мл 1-5%-ного раствора глюкозы и 2,5 мл раствора уксуснокислого фенилгидразина. Пробирку с реакционной смесью помещают на 20-30 минут в кипящую водяную баню. Выпадает осадок глюкоозазонов, количество которого увеличивается при встряхивании и охлаждении реакционной смеси. Уксуснокислый фенилгидразин легко гидролизуется, так что в реакцию с глюкозой вступает свободный фенилгидразин.
Напишите уравнения реакций гидролиза уксуснокислого фенилгидразина и взаимодействия глюкозы с избытком фенилгидразина (три стадии). Какие гексозы дают такой же фенилозазон, как и глюкоза?
Опыт 11. Осмоление моносахаридов под действием щелочи.
Реакция основана на общей для альдегидов склонности к образованию в щелочной среде продуктов конденсации (альдегидные смолы).
В пробирку наливают 1 мл 10%-ного раствора глюкозы и добавляют 1 мл концентрированного (30-40%-ного) раствора гидроксида натрия. Нагревают смесь до кипения и кипятят в течение 2-3 минут.
При выполнении опыта необходимо соблюдать осторожность: реакционная смесь кипит толчками и ее может выбросить из пробирки. Жидкость в пробирке желтеет, затем делается бурой и, наконец, темно-бурой. Появляется запах карамели, особенно заметный при подкислении раствора 10%-ной серной кислотой.
Цветные реакции на моносахариды
Опыт 12. Реакция Селиванова на кетогексозы
Реактив Селиванова готовят следующим образом: 50 мл концентрированной соляной кислоты смешивают с 50 мл дистиллированной воды. В 100 мл полученного раствора соляной кислоты растворяют 0,5 г резорцина.
В две пробирки наливают по 2 мл реактива Селиванова и прибавляют по 2 капли 1%-ных растворов глюкозы и фруктозы. Обе пробирки одновременно помещают в водяную баню с температурой воды 80 0 С и выдерживают при этой температуре в течение 8 минут. В пробирке с фруктозой появляется интенсивное красное окрашивание. Глюкоза в условиях опыта окрашивания не дает.
Объясните опыт и напишите уравнения реакций дегидратации фруктозы и конденсации оксиметилфурфурола с резорцином с образованием окрашенных хиноидных соединений.
Источник
Химические свойства фруктозы. Получение. Применение
Фруктоза вступает во все реакции многоатомных спиртов: образует сахараты с нерастворимыми в воде гидроксидами, простые и сложные эфиры. Однако наличие в молекуле вместо альдегидной группы кетонного фрагмента затрудняет реакции окисления фруктозы. Например, глюкоза окисляется бромной водой до глюконовой кислоты, а фруктоза к подобному превращению не способна:
Эта реакция позволяет отличить альдозы от кетоз.
Как и все моносахариды, фруктоза не подвергается гидролизу.
Фруктозу получают гидролизом сахарозы под влиянием сильных кислот или энзимов. При гидролизе одной молекулы сахарозы получается одна молекула глюкозы и одна молекула фруктозы:
Фруктоза применяется в кондитерском деле, используется как подсластитель, применяется в медицине в качестве заменителя сахарозы. В естественном виде, в составе фруктов, овощей и ягод, фруктоза благотворно влияет на организм: снижает воспалительные процессы в полости рта и вероятность развития кариеса на 35 %. Кроме того, моносахарид выступает природным антиоксидантом, продлевает срок годности продуктов, сохраняя их в свежем состоянии. Фруктоза не вызывает аллергии, хорошо усваивается организмом, препятствует накоплению лишних углеводов в тканях, снижает калорийность пищи и ускоряет восстановление после умственного, физического напряжения. Соединение проявляет тонизирующие свойства, поэтому его рекомендуют употреблять людям с активным образом жизни, спортсменам. Фруктоза используется в кулинарии как заменитель сахара, консервант и усилитель ягодного аромата при изготовлении следующей продукции: молочных изделий; сладких напитков; выпечки; варенья; десертов с пониженной калорийностью; ягодных салатов; мороженного; консервированных овощей, фруктов; соков; джемов; сладостей для диабетиков (шоколада, печенья, конфет).
Задача. Вещество имеет следующий состав:
Источник
Лекция Углеводы. Химические свойства
Химические свойства моносахаридов обусловлены наличием:
- карбонильной группы (ациклическая форма моносахарида)
- полуацетального гидроксила (циклическая форма моносахарида)
- спиртовых ОН групп
Восстановление
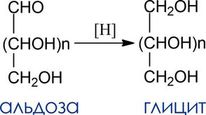
- Продукты восстановления: многоатомные спирты –глициты
- Восстановитель: NaBH4 или каталитическое гидрирование.
Глициты используются в качестве заменителей сахара.
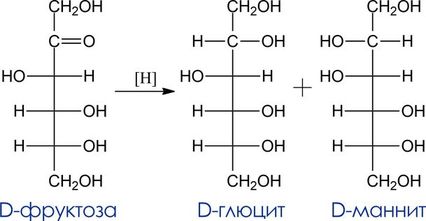
При восстановлении альдоз происходит “уравнивание” функциональных групп на концах цепи. В результате из некоторых альдоз (эритрозы, рибозы, ксилозы, аллозы, галактозы) образуются оптически неактивные мезо-соединения, например. При восстановлении кетоз из карбонильной группы возникает новый хиральный центр и образуется смесь неравных количеств диастереомерных спиртов (эпимеров по С2):
Эта реакция доказывает, что D-фруктоза, D-глюкоза и D-манноза имеют одинаковые конфигурации хиральных центров С2, С3, и С4.
Окисление
Окислению могут подвергаться:
- карбонильная группа
- оба конца углеродной цепи (карбонильная группа и гидроксогруппа у шестого атома углерода)
- гидроксогруппа у шестого атома углерода независимо от карбонильной
Вид окисления зависит от природы окислителя.
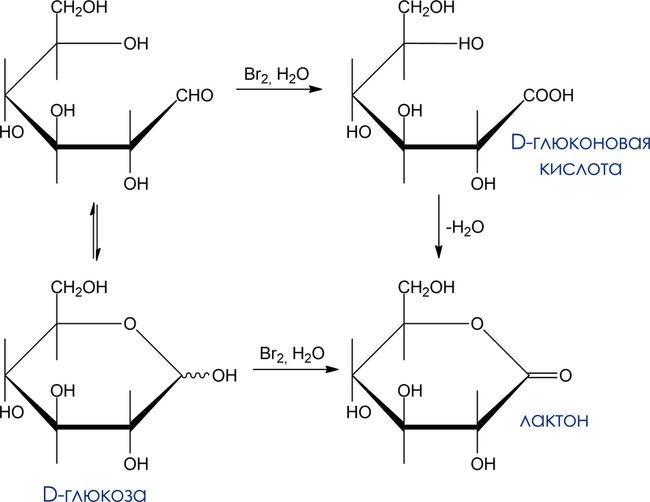
Мягкое окисление. Гликоновые кислоты
- Окислитель: бромная вода
- Что окисляется: карбонильная группа альдоз. Кетозы в этих условиях не окисляются и могут быть таким образом выделены из смесей с альдозами.
- Продукты окисления: гликоновые кислоты (из ациклических моносахаридов), пяти- и шестичленные лактоны (из циклических).
Восстанавливающие моносахариды. Качественная реакция на альдегидную группу
- Окислитель: катионы металлов Ag + ([Ag(NH3)2]OH – реактив Толенса) и Cu 2+ (комплекс Cu 2+ с тартрат-ионом – реактив Фелинга) в щелочной среде
- Что окисляется: карбонильная группа альдоз и кетоз
- Продукты окисления: гликоновые кислоты и продукты деструктивного распада
Альдоза + [Ag(NH3)2] + → гликоновая кислота + Ag + продукты деструктивного окисления
Альдоза + Cu 2+ → гликоновая кислота + Cu2O + продукты деструктивного окисления
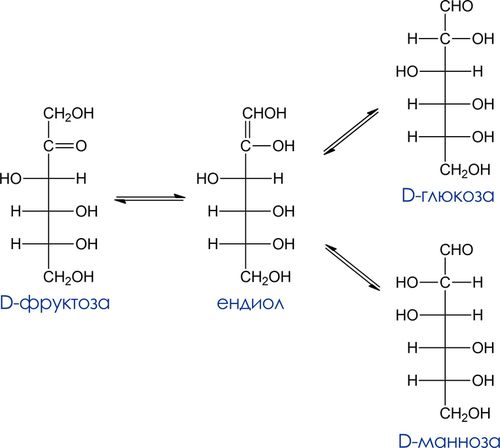
Восстанавливающие углеводы – углеводы, способные восстанавливать реактивы Толенса и Фелинга. Кетозы проявляют восстанавливающие свойства за счет изомеризации в щелочной среде в альдозы, которые и взаимодействуют далее с окислителем. Процесс превращения кетозы в альдозу происходит в результате енолизации. Образующийся из кетозы енол является общим для нее и 2-х альдоз (эпимеров по С-2). Так, в слабощелочном растворе в равновесии с D-фруктозой находятся ендиол, D-глюкоза и D-манноза.
Эпимеризация – взаимопревращения между альдозами, эпимерами по С2 в щелочном растворе.
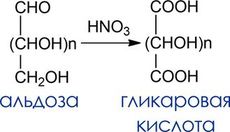
Жесткое окисление. Гликаровые кислоты
- Окислитель: разбавленная азотная кислота
- Что окисляется: оба конца углеродной цепи. Окисление кетоз азотной кислотой протекает с расщеплением С-С связей.
- Продукты окисления: гликаровые кислоты
При образовании гликаровых кислот, происходит “уравнивание” функциональных групп на концах цепи и из некоторых альдоз образуются мезо-соединения.
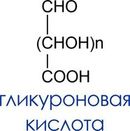
Ферментативное окисление в организме. Гликуроновые кислоты
- Окислитель: ферменты в организме. В лабораторных условиях для защиты карбонильной группы проводят многостадийный синтез.
- Что окисляется: гидроксогруппа у шестого атома углерода независимо от карбонильной
- Продукты окисления: гликуроновые кислоты
Гликуроновые кислоты входят в состав полисахаридов (пектиновые вещества, гепарин). Важная биологическая роль D-глюкуроновой кислоты состоит в том, что многие токсичные вещества выводятся из организма с мочой в виде растворимых глюкуронидов.
Реакции полуацетального гидроксила. Гликозиды
Моносахариды способны присоединять соединения различной природы с образованием гликозидов. Гликозид – молекула, в которой остаток углевода связан с другой функциональной группой посредством гликозидной связи.
В присутствии кислот моносахариды взаимодействуют с соединениями, содержащими гидроксогруппу. В результате образуются циклические ацетали – O-гликозиды.
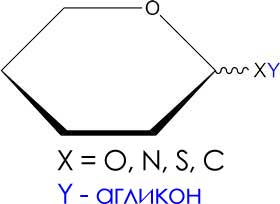
Строение гликозидов
Молекула гликозида состоит из двух частей – углеводная компонента и агликон:
По типу связи углеводного остатка и агликона различают:
По размеру цикла гликозиды:
- глюкозиды (ацетали глюкозы)
- рибозиды (ацетали рибозы)
- фруктозиды (ацетали фруктозы)
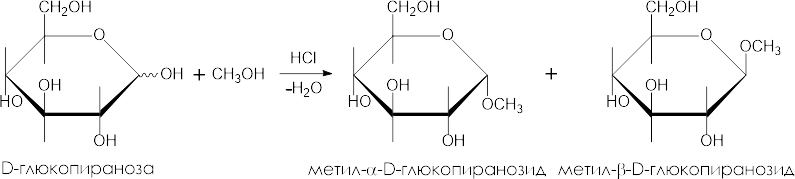
Получение гликозидов
Распространенный способ получения гликозидов – пропускание газообразного хлороводорода (катализатор) через раствор моносахарида в спирте:
Гидролиз гликозидов
Гликозиды легко гидролизуются в кислой среде, устойчивы к гидролизу в слабощелочной среде. Фуранозиды из-за напряженности цикла гидролизуются легче пиранозидов. В результате гидролиза гликозидов образуется соответствующее гидроксосодержащее соединение (спирт, фенол и т. д.) и моносахарид.
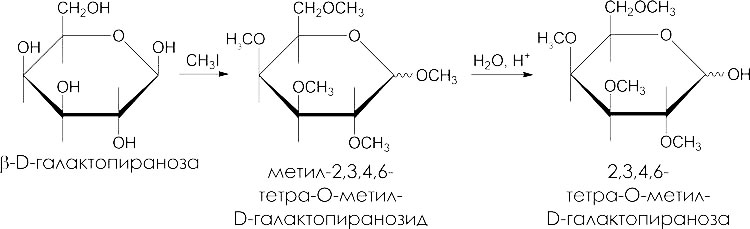
Образование простых эфиров
При взаимодействии спиртовых гидроксогрупп с алкилгалогенидами образуются простые эфиры. Простые эфиры устойчивы к гидролизу, а гликозидная связь гидролизуется в кислой среде:
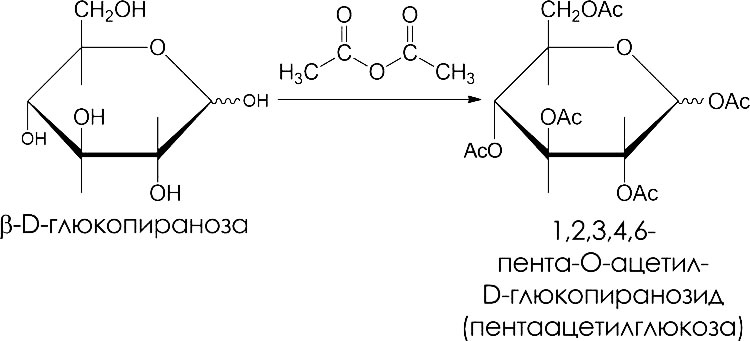
Образование сложных эфиров
Моносахариды вступают в реакцию ацилирования с ангидридами органических кислород. В результате образуются сложные эфиры. Сложные эфиры гидролизуются как в кислой, так и в щелочной средах:
Дегидратация
Дегидратация углеводов происходит при нагревании с минеральными кислотами:
Источник