Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Внимание, если вы не нашли в базе сайта нужную реакцию, вы можете добавить ее самостоятельно. На данный момент доступна упрощенная авторизация через VK. Здесь вы можете выбрать параметры отображения органических соединений. Эти параметры действуют только для верхнего изображения вещества и не применяются в реакциях.
Корректная работа сайта обеспечена на всех браузерах, кроме Internet Explorer. Если вы пользуетесь Internet Explorer, смените браузер. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Источник Углеводы. Моносахариды. Принципы строения и химического поведения моносахаридов , страница 4Химический смысл этого явления заключается в том, что каждый твердый препарат моносахарида, представляющий собой какую-либо одну циклическую (полуацетальную) форму, при растворении и стоянии раствора переходит через открытую (ациклическую) оксо-форму в другие циклические формы до достижения состояния равновесия.
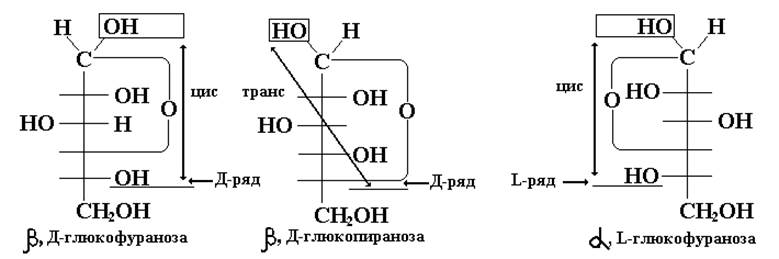
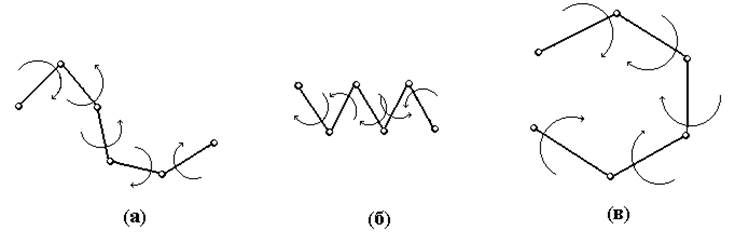
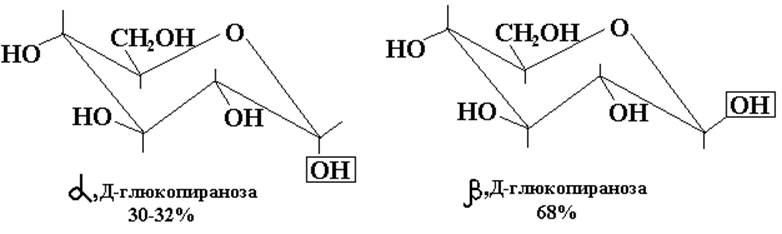
После достижения равновесия в растворе присутствуют все формы данного моносахарида, из которых более устойчивыми для гексоз являются пирановые (шестичленные) циклы, а для пентоз – фурановые (пятичленные) циклы. Минимальное содержание в равновесной смеси имеют ациклические (открытые) формы моносахарида. Эти превращения,происходящие в водных растворах со всеми моносахаридами, являются таутомерными превращениями (греч. tauto- тот же самый) и носят название цикло-цепной или оксо-гидрокси-таутомерии. Таутомерия лежит в основе множественности химических свойств моносахаридов. Причем важно не абсолютное содержание того или иного таутомера, а возможность их перехода друг в друга, что приводит к пополнению количества «нужной» формы по мере ее расходования в каком-либо процессе. Образующиеся в результате цикло-цепной таутомерии циклические формы моносахарида называются аномерами (от греч. ана – венх), так как при обычном вертикальном изображении формул моносахаридов (формулы Колли-Толленса) эти формы отличаются конфигурациями у верхнего (первого у альдоз) углеродного атома. α-аномером называется та циклическая форма, у которой полуацетальный (аномерный) гидроксил расположен в цис-положении относительно гидроксила, определяющего ряд моносахарида; β-аномер имеет транс-расположение полуацетального (аномерного) гидроксила и гидроксила, определяющего ряд. Более совершенный способ изображения циклических форм углеводов был предложен Хеуорсом. В отличие от формул Колли-Толленса, формулы Хеуорса представляют собой пяти- или шестиугольники, в которых аномерный (первый у альдоз) атом расположен справа от атома кислорода. При переходе от формул Колли-Толленса к формулам Хеуорса следует помещать под цикл все атомы и функциональные группы, стоящие справа у атомов углерода, входящих в цикл, в формулах Колли-Толленса. Атомы углерода, не вошедшие в цикл, располагаются сверху в формулах Хеуорса (только для Д-ряда). Правила перехода к формулам Хеуорса для L-ряда более сложные. Например, β-, Д-фруктофураноза: Молекулы моносахаридов, находящиеся в ациклической (оксо-) форме, благодаря возможности вращения вокруг простых -связей, постоянно изгибаются, принимая различные хаотические (а), зигзагообразные (б), и клешневидные (в) конформации. Клешневидная конформация приводит к пространственному сближению двух реакционно способных групп (=О) и (-ОН) и образованию циклических форм (циклических полуацеталей), среди которых устойчивы и существуют только пяти- и шестичленные циклы. Шестичленные циклы, подобно циклогексану,наиболее устойчивы в конформации «кресло». Причем из двух пирановых аномеров глюкозы наиболее устойчив β-аномер, имеющий экваториальное положение всех заместителей. Эпимерами называются стереоизомеры моносахаридов,отличающиеся конфигурациейтолько одного хирального центра. Эпимеры, таким образом, являются частным случаем диастереомеров. Аномеры, в свою очередь, являются частным случаем эпимеров, так как различаются всегда только конфигурациейаномерного хирального центра. Эпимеры же в общем понятии могут различаться любым, но только одним хиральным центром. Источник |

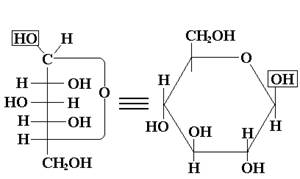
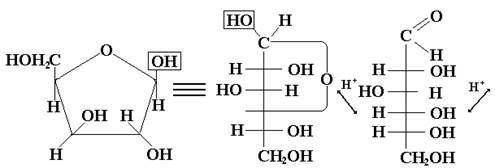
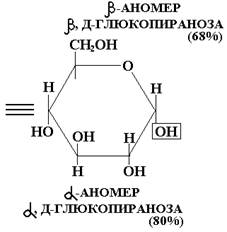
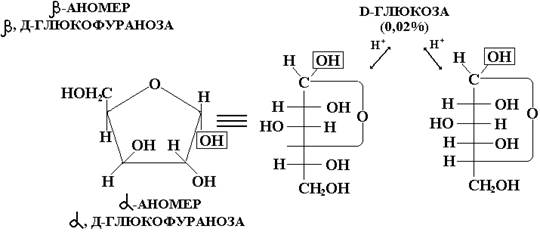 5-членные фурановые циклы 6-членные пирановые циклы
5-членные фурановые циклы 6-членные пирановые циклы